Lovande resultat med panitumumab i tillägg till neoadjuvant kemoterapi vid kolorektalcancer
En förstärkt trend till förbättrad återfallsfri överlevnad i och med signifikant förbättrad sjukdomsfri överlevnad och lägre risk för cancerspecifik död. Det är resultatet av tillägg av Vectibix till neoadjuvant kemoterapi för patienter med operabel tjocktarmscancer av RAS/BRAF-vildtyp.

Den nya analysen från FOxTROT-studien presenterades på den nyligen avslutade ESMO-kongressen i Madrid. Foto: Åsa Sandin.
– Behandlingen visar lovande aktivitet, och när den ges till rätt patienter tycks den ha effekt på överlevnad, säger Daniel Brattström, överläkare vid sektionen för GI-cancer, Tema Cancer, på Karolinska Universitetssjukhuset, Stockholm.
Den nya analysen från FOxTROT-studien presenterades på ESMO-kongressen i Madrid.
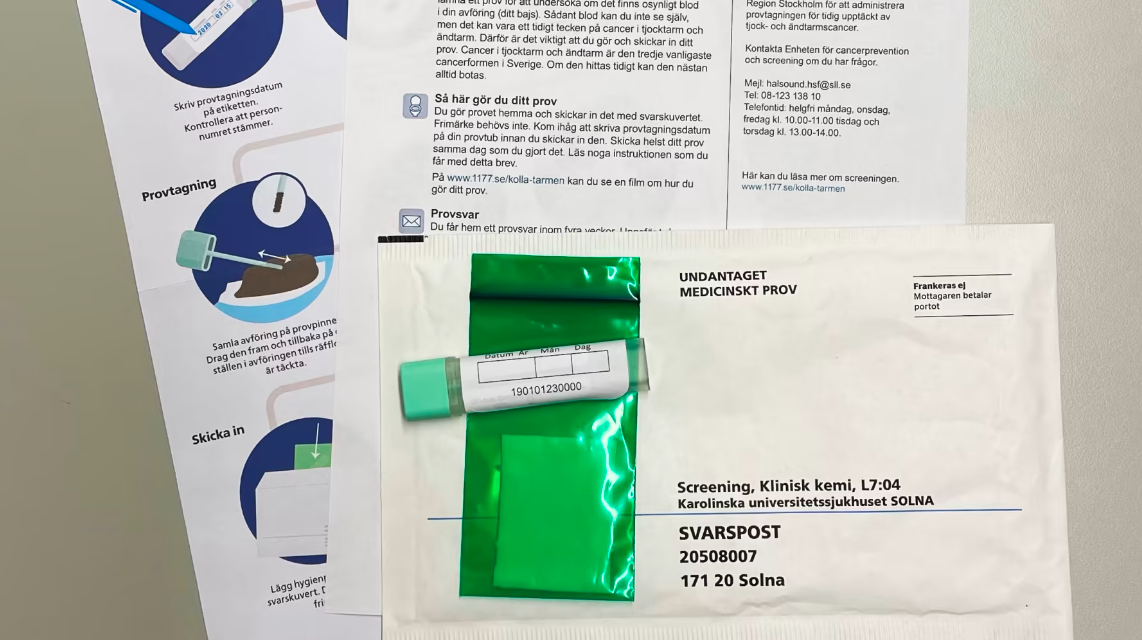
Kolorektalcancer är världens näst vanligaste form av cancer. Standardbehandlingen är kirurgi, ibland följt av adjuvant behandling med cytostatika. Men trots adjuvant behandling återfaller 20–30 procent av patienterna i sjukdom som vanligtvis är obotlig.
Så sent som i mars i år publicerades en artikel i Journal of Clinical Oncology där man konstaterade att ”endast sex veckors preoperativ oxaliplatin-fluoropyrimidin-kemoterapi för operabel tjocktarmscancer kan ges säkert utan att öka perioperativ morbiditet. Denna kemoterapiregim, när den ges preoperativt, ger markant histopatologisk downstaging [minskning av tumörvolym], färre ofullständiga resektioner och bättre sjukdomskontroll efter två år”. Här kunde patienter med RAS-vildtyptumörer randomiseras till att få tillägg av Vectibix (panitumumab) till neoadjuvant kemoterapi. Det primära effektmåttet för subrandomiseringen, djupet av extramural tumörutbredning, nåddes emellertid inte då skillnaden inte var signifikant.
Till den analys som nu presenterats på ESMO har forskarna lagt en utökad biomarkörstestning. Biomarkörsdata fanns tillgänglig för 232 (83 procent) av de randomiserade patienterna. Med hjälp av NGS, Next Generation Sequencing, kunde man då se att 22 (9,5 procent) av dessa hade RAS-mutation och 41/210 (19,5 procent) hade BRAF-mutation – alltså mutationer som är associerade med sämre svar på anti-EGFR-behandling, något som potentiellt påverkat de tidigare resultaten.
Efter en medianuppföljning på 42 månader av de 169 patienter som hade RAS/BRAF-vildtyp kunde man se att 88,1 procent av dem som fått tillägg av panitumumab nådde återfallsfri överlevnad (RFS = Recurrence-Free Survival) medan motsvarande andel bland dem som enbart fått FOLFOX var 79,5 procent.
– Troligen hade signalen rörande återfallsfri överlevnad varit än mer tydlig ifall man analyserat tillägg av panitumumab i mer avancerade stadier, säger Daniel Brattström.
Trots att tillägg av panitumumab inte resulterade i större patologisk respons eller minskning av tumörvolym jämfört med enbart FOLFOX, ledde tillägget ändå till en förbättring ifråga om koloncancerspecifik överlevnad.
– Det här är en explorativ analys som genererar intressanta hypoteser och visar på potentialen av att selektera patienter till en viss behandling utifrån biomarkörstatus, säger Daniel Brattström.
Forskarna bakom studien noterar att, med undantag för checkpointhämmare till patienter med hög mikrosatellitinstabilitet, är detta första gången ett biologiskt läkemedel visar effekt vid neoadjuvant behandling av kolorektalcancer.
Panitumumab-behandling var associerad med högre frekvens av grad 3 diarré (8 % vs 3 %) och utslag (22 % vs 2 %) jämfört med enbart FOLFOX. En icke signifikant ökning i antalet postoperativa komplikationer, anastomosläckage och abscessutveckling, syntes också (8,6 % vs 3,1 %). Inga postoperativa komplikationer av tillägget föranledde förlängda sjukhusvistelser.