Tagrisso godkänt i EU för adjuvant behandling vid EGFR-muterad lungcancer i tidigt stadium
Godkännandet baseras på resultat från fas III-studien ADAURA där Tagrisso minskade risken för återfall med 80%.
Denna webbsida är endast avsedd för läkare och sjukvårdspersonal med förskrivningsrätt.
Godkännandet baseras på resultat från fas III-studien ADAURA där Tagrisso minskade risken för återfall med 80%.
AbbVie, ett forskande biopharmaföretag, meddelar att EU-kommissionen har godkänt Venclyxto i kombination med hypometylerande läkemedel, azacitidin eller decitabin, för behandling av vuxna nydiagnostiserade AML-patienter, som inte är lämpliga för intensiv kemoterapi.1 Godkännandet gäller i alla 27 EU-länderna, liksom Island, Liechtenstein och Norge.
– EU-kommissionens godkännande av venetoklax kombinationsbehandling är ett viktigt framsteg inom AML och medför ett nytt behandlingsalternativ för personer som står inför vad som ofta är en förödande akut leukemidiagnos, säger Zack Pemberton-Whiteley, ordförande i Acute Leukemia Advocates Network.
Fullständigt globalt pressmeddelande, inklusive referenser återfinns här.
Amgen presenterar data från ett flertal studier ur sin ständigt växande onkologi-portfölj när ASCO, världens viktigaste onkologikonferens, slår upp sina virtuella portar den 4 juni. Det gäller såväl uppdateringar om etablerade terapier som Amgens innovativa pipeline med bland annat KRASG12C-hämmaren sotorasib vid lungcancer, och bemarituzumab vid esofagus- och ventrikelcancer.
– På de senaste ASCO-mötena har det blivit allt tydligare att det är precisionsmedicin som banar väg för framtidens cancervård, och Amgen fortsätter att bryta ny mark genom att utforska målriktade behandlingsmetoder för patienter med svårbehandlade cancerformer, säger Sandra Eketorp Sylvan, onkolog och medicinsk chef för Amgen Sverige.
En av de substanser i Amgens onkologi-pipeline som väckt mest intresse på senare tid är sotorasib, den första KRASG12C-hämmaren som nått klinisk fas. Mot bakgrund av att denna mutation länge ansetts i det närmaste omöjlig att påverka med läkemedel har de hittills presenterade resultaten väckt hoppet om en första målriktad behandling för de cirka 13 procent av patienter med icke-småcellig lungcancer (NSCLC) vars tumörer är KRASG12C-positiva.
Vid en muntlig session på fredagen presenteras för första gången data för total överlevnad (OS) för sotorasib från fas II-studien CodeBreaK 100. I samband med detta tillkännages även resultaten av biomarköranalyser i subgrupper.
Vid en annan muntlig session presenteras uppdaterade data från fas II-studien FIGHT där bemarituzumab, en monoklonal antikropp riktad mot FGFR2b, i kombination med kemoterapi (modifierad FOLFOX6) utvärderas vid behandling av patienter med avancerad FGFR2b-positiv esofagus- och ventrikelcancer (GEJ = gastric and gastroesophageal junction adenocarcinoma).
– Vi vet sedan tidigare att den här kombinationen givit statistiskt signifikanta förbättringar av progressionsfri överlevnad, total överlevnad och responsfrekvens jämfört med enbart FOLFOX6, säger Sandra Eketorp Sylvan.
På ASCO presenteras också uppdaterade säkerhets- och effektdata från first-in-human-studien av AMG 757 (tarlatamab) vid småcellig lungcancer (SCLC). Tarlatamab är en BiTE-molekyl med förlängd halveringstid som riktas mot DLL3 (delta-like ligand 3), vilket aktiverar den cytotoxiska potentialen hos T-celler för att bekämpa neuroendokrin cancer såsom småcellig lungcancer och neuroendokrin prostatacancer.
Vidare presenteras data från prövarinitierade studier på Vectibix (panitumumab) vid metastaserad kolorektalcancer (mCRC), bland annat PanaMa-studien som utvärderar Vectibix i kombination med 5-fluorouracil/leukovorin (5FU/LV) som underhållsbehandling och nya data från studien CHRONOS som utvärderar Vectibix som rechallenge therapy.
16 juni 2021, kl. 16.00-16.45
Fokus på urotelial cancer – Post ASCO
Paneldiskussion
Föreläsare:
Överläkare onkolog Lennart Åström, Kirurgkliniken, Halmstad
Överläkare patolog Anca Dragomir, Klinisk patologi, Akademiska sjukhuset, Uppsala
Överläkare urolog Petter Kollberg, Urologiska kliniken, Helsingborg
Merck och Pfizer har nöjet att bjuda in till webinar med fokus på urotelial cancer.
Onkolog Lennart Åström kommer att presentera en sammanfattning av data inom urotelial cancer från ASCO. Efter presentationen öppnas det upp för en paneldiskussion där patolog Anca Dragomir och urolog Petter Kollberg ansluter för att diskutera presenterade data ur ett kliniskt perspektiv. Möjlighet finns till interaktivitet under webinaret.
Webinaret hålls på svenska och är avsett för personal inom Hälso- och Sjukvård (HCP).
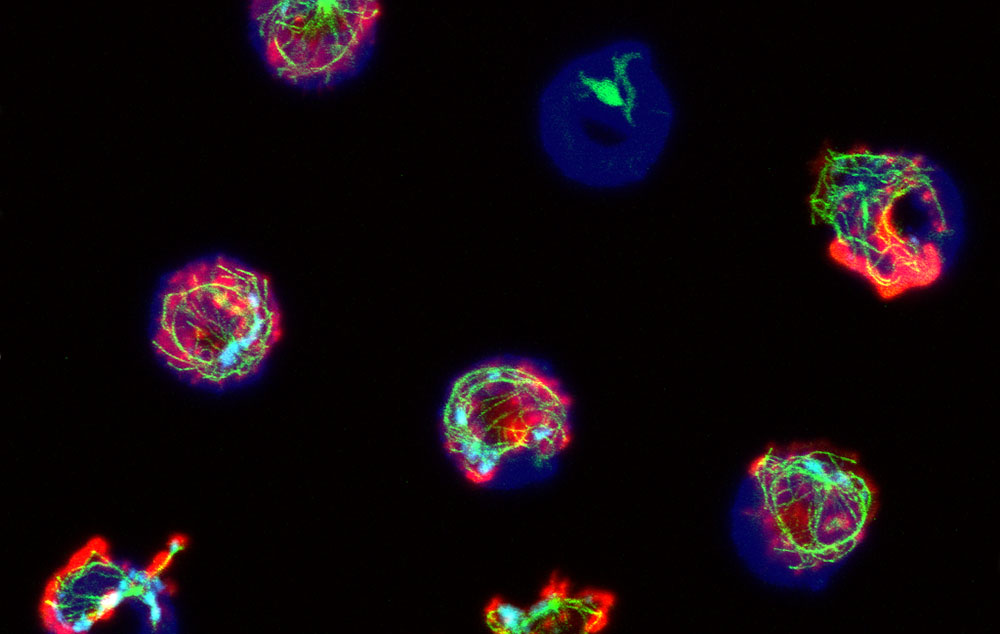 ”Med hjälp av högupplöst fluorescensmikroskopi har vi studerat hur enskilda NK-cellers svar mot olika tumörcellsliknande stimuli skiljer sig åt. Sådan forskning kan hjälpa oss att förstå hur sjuka celler kan undgå att upptäckas av immunförsvaret, säger Quentin Verron, en av forskarna bakom arbetet.
”Med hjälp av högupplöst fluorescensmikroskopi har vi studerat hur enskilda NK-cellers svar mot olika tumörcellsliknande stimuli skiljer sig åt. Sådan forskning kan hjälpa oss att förstå hur sjuka celler kan undgå att upptäckas av immunförsvaret, säger Quentin Verron, en av forskarna bakom arbetet.
En grupp forskare från KTH har studerat det mänskliga immunförsvaret och de celler som är aktiva för att skydda oss från infektioner och cancer. Arbetet har lett till nya idéer om hur sjuka celler kan undvika att bli upptäckta och dödade, det vill säga påverka immunförsvaret negativ så att det inte fungerar.
Forskargruppen, där bland andra Björn Önfelt som är professor i tillämpad fysik vid KTH ingår, har arbetat med att öka förståelsen för immunförsvarets celler och deras funktioner. Här ingår NK- (natural killer) och cytotoxiska T-celler, som känner igen och dödar sjuka celler. En ökad kunskap kan bidra till att det går att påverka cellerna genom biologiska läkemedel.
Oklara mönster
När NK- och T-celler känner igen och dödar sjuka celler sker det genom en så kallad immunologisk synaps, en tajt kontaktyta mellan immun- och målceller. I synapsen samlas ytreceptorer, signaleringsmolekyler och det maskineri som immuncellerna kan använda för att döda målcellen. Proteiner i synapsen organiserar sig ofta i karakteristiska mönster och trots att synapsen studerats av forskare över 20 år är det fortfarande oklart vad dessa mönster har för funktion.
– Vi har studerat processen när NK-celler känner igen de här mönstren. Ett artificiellt system baserat på metoden ”Microcontact printing” har gjort det möjligt att skapa mönster av målcellsproteiner på glasytor. I sin tur har det gjort att vi kunnat studera NK-cellers reaktion, det vill säga igenkänning, synapsbindning och dödande, säger Björn Önfelt
.
Björn Önfelt, professor i tillämpad fysik vid KTH
Sjuka celler kan komma undan
Studien visar bland annat att det sista steget i processen, själva dödandet, hämmas vid ett av mönstren. Ett som är munkliknande (format som en donut). Detta tyder på målceller (de som är sjuka) skulle kunna skydda sig genom att omfördela sina proteiner vid synapsbildning.
Men varför vill de här sjuka cellerna undkomma upptäckt?
– Jag skulle vilja vända på det. Sjukdom uppstår för att cellerna lyckas undvika upptäckt av någon anledning. Det finns förstås en mängd olika anledningar och mekanismer för det, men det klassiska är att immuncellerna saknar nödvändiga receptorer för att upptäcka de sjuka cellerna. De nya resultaten antyder att sjuka celler kan komma undan trots att de bär de ytproteiner som immunförsvaret aktiveras av.