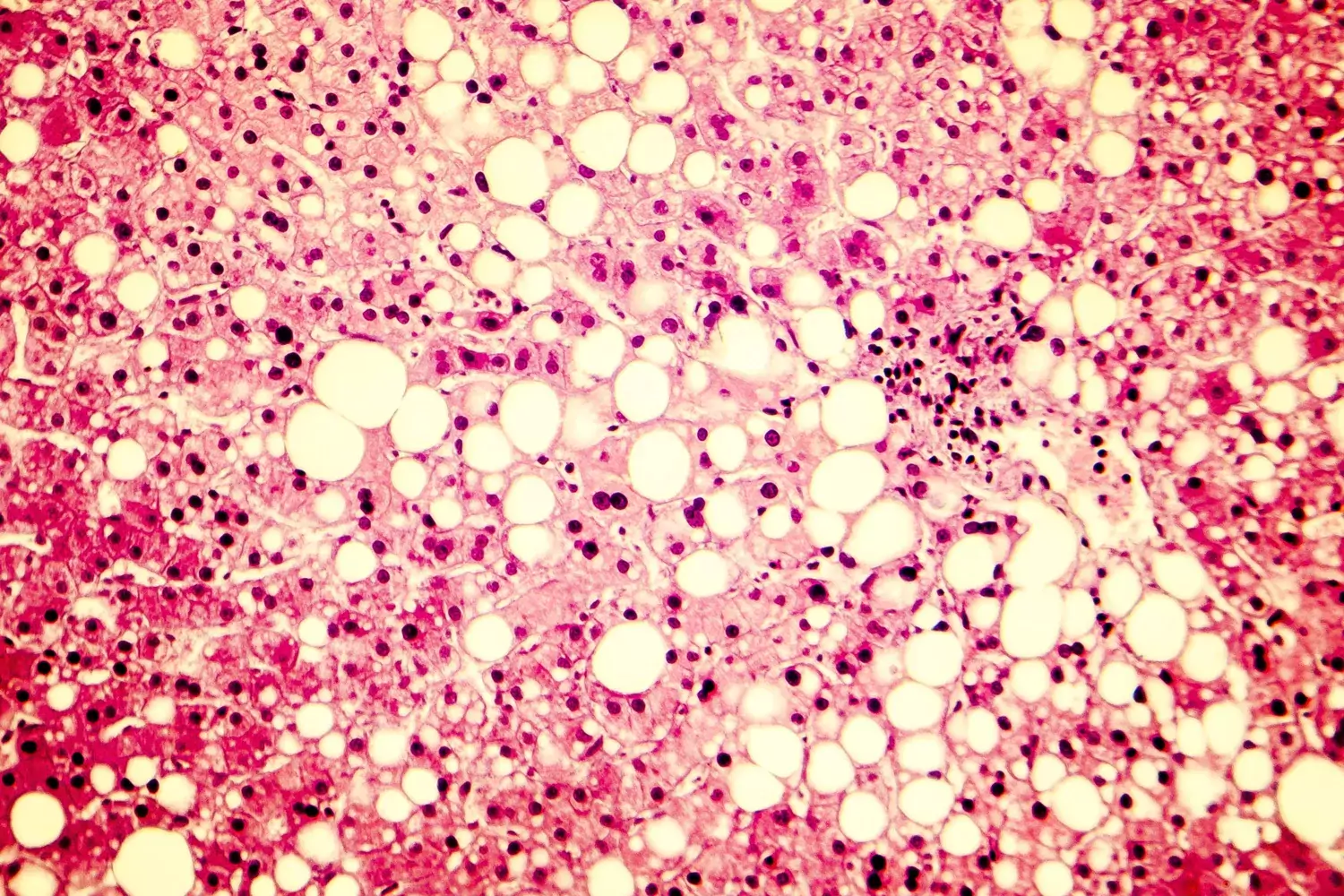
Även familjemedlemmar till personer med metabolt orsakad fettlever har en ökad risk att utveckla levercancer och avlida av leverrelaterade sjukdomar. Detta skulle kunna innebära att även närstående är betjänta av de livsstilsråd som idag endast ges till patienter. Det menar forskare vid Karolinska Institutet som kan visa sambandet i en rikstäckande studie publicerad i Journal of Hepatology.
Personer med metabolt orsakad fettlever har en förhöjd risk att utveckla och avlida i levercancer. Fettlever är idag den främsta orsaken till att levercancer ökar snabbt. Men nu visar forskare vid Karolinska Institutet att även nära släktingar och partners har en förhöjd risk att drabbas av leverrelaterade sjukdomar.
Bör utvärdera nyttan med screening
– Patienter med metabolt orsakad fettlever bör inte behandlas isolerat utan rekommendationer om livsstilsförändringar bör ges till både släkt och familj. Dessutom talar vår studie för att man bör utvärdera nyttan med screening av nära släktingar med ytterligare riskfaktorer, säger studiens försteförfattare Fahim Ebrahimi, läkare och forskare vid institutionen för medicinsk epidemiologi och biostatistik, Karolinska Institutet.
Forskarna har använt sig av den så kallade ESPRESSO-kohorten som bland annat innehåller information om alla leverbiopsier tagna i Sverige från 1965 och framåt. Där fann de knappt 12 000 personer med biopsiverifierad MASLD (”Metabolic dysfunction-associated steatotic liver disease”, tidigare kallat NAFLD, se faktaruta). Till var och en av dessa matchades upp till fem kontrollpersoner. Därefter identifierades nära släktingar (föräldrar, syskon och barn) till båda grupperna liksom partners. Totalt omfattar studien närmare 250 000 nära släktingar och 57 000 partners.
Följdes i upp till 50 år
Med en uppföljningstid på, i snitt, 17,6 år, där vissa individer följdes så länge som 50 år, fann forskarna att nära släktingar till MASLD-patienter löpte en 80 procent ökad risk att drabbas av levercancer jämfört med kontrollerna. Men levercancer är en relativt ovanlig sjukdom vilket gör att den absoluta riskökningen att drabbas är betydligt lägre. Enligt forskarna är den absoluta riskökningen under 20 års tid 0,11 procent.
– Det innebär att ytterligare en av 900 nära släktingar till patienter med MASLD utvecklar levercancer under en 20-årsperiod. Så den absoluta risken är liten. Men på populationsnivå är den ändå relevant, säger studiens sisteförfattare Jonas F. Ludvigsson, professor vid institutionen för medicinsk epidemiologi och biostatistik, Karolinska Institutet.
Miljöfaktorer spelar in
Partners till MASLD-patienterna hade klart förhöjda risker att drabbas av allvarlig leversjukdom som till exempel cirros (skrumplever) och död.
– Detta bekräftar att det finns en tydlig ärftlighet i metabolt orsakade fettleversjukdomar, men också att miljöfaktorer, som en delad livsstil, spelar en viktig roll, säger Fahim Ebrahimi.
Forskningen finansierades av Swiss National Science Foundation (SNSF) och Karolinska Institutet. Fahim Ebrahimi, Hannes Hagström och Jonas F. Ludvigsson har alla haft ekonomiska relationer till olika läkemedelsbolag, främst i form av forskningsstöd för andra, orelaterade, studier, men även för rådgivande funktioner.