Region Skåne inför nu helgenomsekvensering som rutindiagnostik vid barncancer men arbetar också för nya screening- och uppföljningsprogram utifrån den genetiska information som analyserna ger. Målet är att hitta barn som riskerar att drabbas av cancer eller canceråterfall tidigare, innan sjukdomen bryter ut.

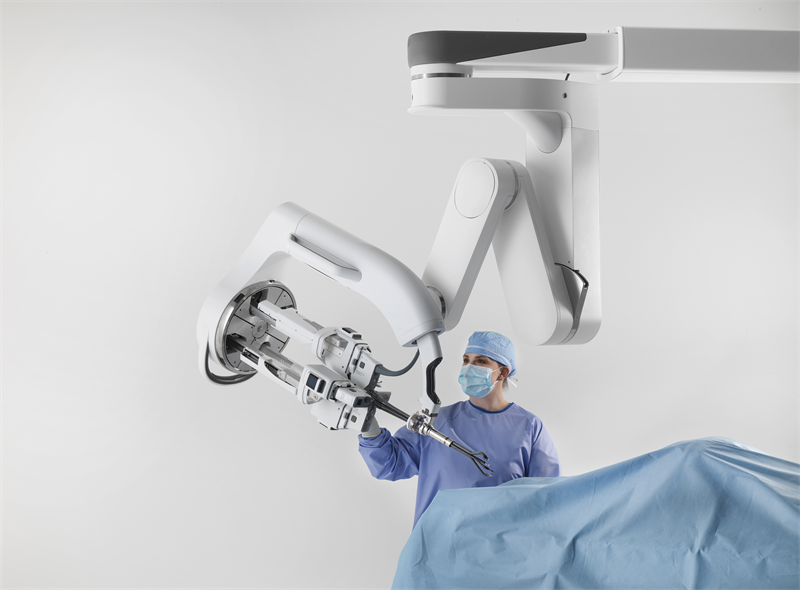
Region Skåne tar över finansieringen av helgenomsekvensering och inför det som rutindiagnostik för cancerdrabbade barn.
Nu meddelar Region Skåne, liksom tidigare Norra sjukvårdsregionen, att de tar över finansieringen av de genetiska diagnoser som tills nu finansierats via projektet GMS barncancer. Stefan Jovinge, Forskning- och undervisningschef Skånes universitetssjukhus tyckte inte att det var ett svårt beslut.
– Helgenomskevensering som diagnosmetod för barncancer har visat sin styrka, särskilt när vi väger in den snabba utvecklingen inom precisionsmedicinen. Vi har redan idag fall där tumörens arvsmassa styr behandlingen så helgenomsekvensering blir allt viktigare inom onkologin.
Stefan Jovinge berättar att Region Skåne och Region Stockholm har störst sekvenseringskapacitet i landet. Han menar också att barnonkologin ligger långt framme inom området genetiska analyser tack vare arbetet inom GMS barncancer, och att det kommer att komma till nytta även för andra patientgrupper och andra sjukdomsområden.
– Vi har i regionen gjort stora satsningar på ny utrustning för sekvensering och vi har också nyligen satsat stort på ett precisionsmedicinskt centrum, ATMP-center. Där kan vi redan idag ge genterapibehandlingar och bota sjukdomar som det tidigare inte fanns behandlingar för men vi kommer också att kunna ta fram helt nya precisionsläkemedel och immunterapier.
Onkogenetik framväxande område
Helgenomsekvensering öppnar också upp för utveckling av cancerprevention och screeningprogram inom barnonkologin. Joakim Wille, läkare och barnonkolog på Barncancercentrum vid Skånes Universitetssjukhus, är lokalt ansvarig för ett delprojekt av GMS Barncancer som kallas ChiCAP, Childhood Cancer Predisposition study. Inom GMS Barncancer studerar man gener för att kunna sätta en precis diagnos och se om det finns någon passande behandling mot någon av de identifierade mutationerna. Inom ChiCAP så studerar man ytterligare 200 gener som sedan tidigare är kända för att kunna påverka utvecklingen av barncancer, så kallad cancerpredisposition. Kartläggningen av dessa medfödda mutationer kallas onkogenetik och Joakim Wille bygger nu upp den onkogenetiska verksamheten i Lund. Han har också startat ett nationellt nätverk av barnonkologer som ska garantera att alla barn som har en predisposition för cancer ska behandlas lika.
– Förutom barn redan drabbade av cancer så kan det handla om både symptomfria och till synes friska barn som vi vet bär på en mutation då föräldrar eller syskon insjuknat. Dessa barn vill vi följa, kunna erbjuda screening och uppföljning som möjliggör tidig upptäckt när väl en cancer utvecklas.
Vissa barncancerprotokoll, de riktlinjer som styr behandlingen av olika diagnoser, är redan idag anpassade för några kända genetiska avvikelser. Joakim Wille hoppas också att de tillstånd hos barn som innebär högre risk för cancer ska inkluderas i arbetet med vårdprogram för ärftlig cancer.
– Det innebär att barnet kan få både ett anpassat behandlingsprotokoll liksom ett anpassat kontrollprogram när vi hittat en sådan här mutation. Och om vi genom screening kan upptäcka och behandla tumörerna tidigare så hoppas vi att vi det kan leda till mindre kirurgiska ingrepp och kanske mindre strålning på grund av metastasbildning vilket vi i sin tur hoppas ska leda till både bättre överlevnad och mindre sena komplikationer orsakade av tuff behandling.
Att Sverige har valt att helgenomsekvensera alla barn som insjuknar i cancer är unikt, i andra länder görs det bara vid vissa diagnoser och återfall. Britt-Marie Frost, forskningschef på Barncancerfonden som också arbetat som barnonkolog i över 30 år ser en lovande utveckling.
– Vi ser en fantastisk kunskapsutveckling just nu och svensk onkogenetik inom barnonkologi ligger i internationell framkant. Vi kommer att kunna införa preventions- och screeningprogram för de barn som har syndrom eller mutationer som innebär en högre risk för att utveckla cancer. Och vi har redan idag exempel på hur det här projektet bidragit till helt ny behandling.
Fakta Södra sjukvårdsregionen:
Varje år insjuknar omkring 55–60 barn i Södra sjukvårdsregionen, i en cancersjukdom.
300–350 barn är under vård eller aktiv uppföljning för en cancersjukdom inom Södra sjukvårdsregionen.
I Södra sjukvårdsregionen finns ungefär 1800–2000 barncanceröverlevare.
Barncancercenter vid Skånes Universitetssjukhus, SUS diagnosticerar och initierar all onkologisk behandling för barn med cancer inom Södra sjukvårdsregionen. Detta inkluderar stamcellstransplantation, som genomförs rutinmässigt.
Mycket av den onkologiska behandlingen sker på Barncancercentrum på SUS, men där det är möjligt erhåller barnen även vissa av onkologiska behandlingar.
SUS har sedan många år tillbaka en väl fungerande Uppföljningsmottagning, som följer vuxna som erhållit onkologisk behandling som barn.
FAKTA GMS Barncancer:
Satsningen inom barncancer startade 2019 med ett uppstartsbidrag från Barncancerfonden på 15 miljoner kronor och görs tillsammans med Barntumörbanken.
Proverna som analyseras samlas in vid Sveriges sex barnonkologiska centrum som ligger i Stockholm, Göteborg, Lund, Uppsala, Linköping och Umeå.
Målet för GMS barncancer är att införa molekylärgenetiska analyser i rutinsjukvården för barn med cancer för att förfina diagnosen och förbättra behandlingsmöjligheterna.
För att GMS Barncancer ska kunna övergå i rutinsjukvården krävs långsiktig finansiering från regionerna.