Fyrsträngat DNA som associeras med uppkomsten av cancer och utveckling av nya cancerläkemedel kan specifikt detekteras med en fluorescerande molekyl. Det visar ett forskarteam vid Umeå universitet i en ny studie som publiceras i Angewandte Chemie.

Erik Chorell, Kemiska institutionen. Nasim Sabouri och Marco Deiana, Institutionen för medicinsk kemi och biofysik. Foto: Ingrid Söderbergh
Forskarna Erik Chorell och Nasim Sabouri och deras forskargrupper vid Umeå universitet har hittat en läkemedelsliknande molekyl som kan användas i cancerceller för att detektera en viss typ av fyrsträngad DNA-struktur, som kallas parallella G-quadruplex DNA-strukturer, G4-DNA.
DNA-molekylerna i människans arvsmassa är uppbyggda av byggstenarna cytosin, guanin, adenin eller tymin och bildar oftast dubbelsträngade spiraler. Men under de senaste decennierna har forskningen visat att det även finns andra alternativa DNA-strukturer i cellen.
Fyrsträngad DNA-struktur bildas när fyra guaninbaser från en DNA-sträng binder till varandra och sedan staplar sig på varandra. G4-DNA finns ofta i närheten av regioner i arvsmassan som slår på aktiviteten av cancerdrivande gener. Detta är en av anledningarna till varför G4-strukturen är ett potentiellt mål för anti-cancerpreparat.
– I vår forskargrupp studerar vi G4-strukturer för att förstå deras biologiska funktion i friska celler och i cancerceller. Vi kan ännu inte med säkerhet säga var i cellen dessa strukturer bildas. Tidigare studier har visat att det bildas fler G4-strukturer i cancerceller än i friska celler och detta är en viktig anledning till varför G4-strukturer är ett mål inom cancerterapin som både vi och andra forskarlag fokuserar på, säger Nasim Sabouri, forskare på Institutionen för medicinsk kemi och biofysik vid Umeå universitet.
Biträdande universitetslektor Erik Chorell och hans forskningsgrupp på Kemiska institutionen vid Umeå universitet arbetar med att designa och utveckla läkemedelslika molekyler som binder till G4-strukturer för att förstå deras funktion och för att utveckla framtida cancerläkemedel. G4-strukturer kan bildas på hundratusentals positioner i den mänskliga arvsmassan så det är helt avgörande att utveckla molekyler som kan binda bara till vissa av dessa.
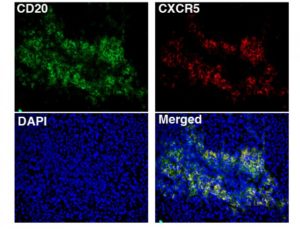
Genom ett långt samarbete har de två forskarlagen nu tillsammans publicerat en vetenskaplig artikel i Angewandte Chemie. I studien har forskarna designat en särskild molekyl som bildar hopfogade aggregat som är svagt fluorescerande. Dessa aggregat omvandlas endast till intensivt fluorescerande monomerer då de binder till en viss typ av G4-struktur men inte när de binder till den dubbelsträngade DNA-spiralen. När ett G4-monomermolekylpar bildas avges en fluorescerande signal som kan detekteras i provröret och inne i cancerceller.
– Vår upptäckt är spännande och motiverande för att fortsätta och fördjupa vår forskning. Molekylen är värdefull som verktyg för unika studier om hur G4-strukturer fungerar och de biologiska processer de är involverade i. Vårt långsiktiga mål är att vidareutveckla våra molekyler mot både cancerdiagnostik och läkemedel, säger Erik Chorell.
Arbetets försteförfattare, Marco Deiana, Institutionen för medicinsk kemi och biofysik, blev rekryterad som postdoktor till Umeå universitet via MIMS Excellence By Choice Postdoctoral Programme för ett år sedan. Programmet har professor Emmanuelle Charpentier som mentor.
Forskarnas vetenskapliga artikel har fått statusen ”highly important”, vilket mindre än 10 procent av de accepterade artiklarna i Angewandte Chemie får.
Text: Ingrid Söderbergh
Om MIMS
MIMS står för Laboratoriet för molekylär infektionsmedicin Sverige (MIMS) inom det nordiska EMBL-partnerskapet för molekylär medicin.
MIMS hemsida
Originalartikel:
Deiana, M., Chand, K., Jamroskovic, J., Obi, I., Chorell, E., och Sabouri, N.: A Light‐up Logic Platform for Selective Recognition of Parallel G‐Quadruplex Structures via Disaggregation‐Induced Emission. Angewante Chemie 2020 (volume 59, Issue 2)