I många år var prostatacancer ett eftersatt forskningsområde trots att prostatacancer är den vanligaste cancersjukdomen. De stora forskningsfinansiärerna prioriterade andra cancersjukdomar. Innan Mustaschkampen fanns så delade Prostatacancerförbundet årligen ut mindre än två miljoner kronor till forskning. Mustaschkampen har bidragit till att uppmärksamheten för behovet av forskning om prostatacancer ökat och gåvorna från företag och allmänheten har ökat så mycket att Prostatacancerförbundet blivit en viktig forskningsfinansiär. De tre senaste åren har förbundet delat ut över 12 miljoner kronor per år till viktiga forskningsprojekt.
– Under de senaste åren har det genomförts många forskningsprojekt som verkligen bidrar till stora viktiga framsteg som till exempel två nya studier vid Karolinska Institutet som påvisar att överdiagnostiken kan minskas väsentligt om personer med förhöjt PSA-värde undersöks med magnetkamera (MR). Detta är ett viktigt steg mot införande av screening, säger Olov Berggren, generalsekreterare Prostatacancerförbundet.
Prostatacancerförbundet har bidragit till att forskningen inom prostatacancer ökar i Sverige, vilket bland annat märks av det ökande antalet ansökningar om forskningsbidrag.
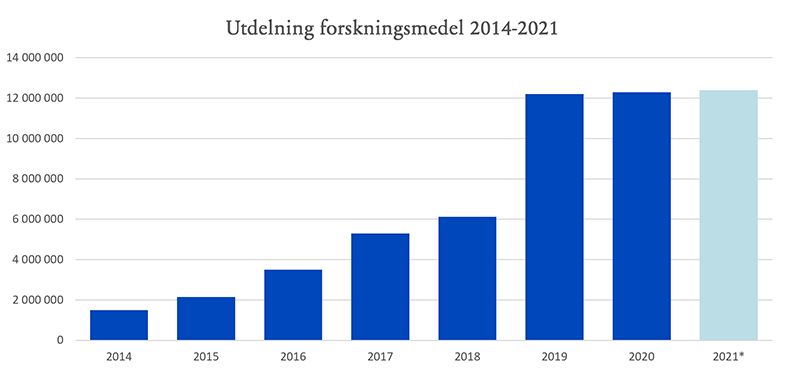
* Utdelade medel hittills under 2021.
Varför är forskning om prostatacancer viktigt?
Prostatacancer är landets vanligaste cancersjukdom och den cancerform som tar flest mäns liv. Tidig upptäckt är avgörande för om sjukdomen ska kunna botas. Forskning pågår för att förbättra diagnostiken och göra den säkrare. Cirka 2 300 avlider varje år av prostatacancer. Spridd cancer innebar förr svårt lidande och snar död. Under de senaste åren har stora framsteg gjorts för att bromsa sjukdomens framfart utan svårare biverkningar. Omfattande forskning pågår för att utveckla nya läkemedel och behandlingsmetoder. På lång sikt anas möjligheten att till och med kunna bota sjukdomen. Prostatacancerförbundet vill driva på detta arbete genom stöd till forskningen. Nedan redovisas några projekt som delvis finansieras av Prostatacancerförbundet.
Anna Lantz, docent och specialistläkare urologi, Karolinska Universitetssjukhuset och en av Mustaschkampens ambassadörer 2021:
Förbättrad uppföljning för män med lågriskprostatacancer
– Jag driver två studier med syftet att förbättra uppföljningen av män med lågriskprostatacancer, STHLM3AS och STHLM3AS-NorDCaP. Målet är att förbättra hur vi idag väljer ut och följer män med lågriskprostatacancer genom att använda en kombination av Stockholm3-testet och magnetkameraundersökning. Den första studien utvärderade 309 män från augusti 2018 till december 2019 och resultaten visar att den nya uppföljningen leder till ökad detektion av behandlingskrävande cancer samtidigt som man minskar behovet av upprepade provtagningar. Nu planerar vi utvidgade analyser, en multicenter valideringsstudie, där vi bjuder in män med lågriskprostatacancer från Norge, Danmark, Finland och Sverige att delta. En implementering av våra resultat på dagens uppföljningsprotokoll kan få viktig inverkan på denna stora grupp av män som går på livslång canceruppföljning, i form av minskad provtagning samt att rätt män väljs ut för behandling.
Utvärdering av nya behandlingsmetoder
– Min tidigare forskning har visat att kirurgisk behandling av prostatacancer är förknippat med stor risk för biverkningar i form av impotens och urinläckage vilket påverkar livskvaliteten. Jag driver nu ett nytt forskningsprojekt med målet att utvärdera en ny behandlingsmetod för lokaliserad prostatacancer, PRIS-studien. Ny bilddiagnostik med magnetkamera har möjliggjort att bättre lokalisera tumörer i prostata och metoder för fokal behandling med mindre risk för sidoeffekter har utvecklats under de senaste årtiondena. Det finns ett flertal olika tekniker som används och tidiga studier har visat att samtliga tekniker har en minskad risk för biverkningar i form av inkontinens och impotens jämfört med konventionell behandling med operation eller strålning. Vårt syfte är att utvärdera fokalbehandling av prostatacancer med IRE teknik med bevarad chans för bot, men där sidoeffekterna och vårdtiden är reducerad jämfört med traditionell behandling. Studien kommer att utföras som ett samarbete mellan sjukhusen i Stockholm och är godkänd av etikprövningsmyndigheten.
Införandet av organiserad prostatacancertestning
– Forskning har visat att prostatacancerscreening med PSA sänker risken för död. Dock har PSA-ledd screening lett till överdiagnostik av icke-behandlingskrävande prostatacancrar och varit den största anledningen till att screening för prostatacancer inte införts, trots att det är vår vanligaste cancerform. Men utvecklingen har gått fort framåt de senaste åren och prostatadiagnostiken har förändrats i grunden, framförallt med utvecklingen av magnetkamerabilder som en del i utredningen. Inom urologin vill vi verka för att förbättra diagnostiken av prostatacancer för att upptäcka alla cancrar i tid, när de fortfarande är botbara. Organiserad prostatacancertestning har redan påbörjats som pilotprojekt i några regioner i Sverige och jag kommer under 2021 delta i arbetsgruppen för att införa detta i Region Stockholm.
Kimia Kohestani, specialistläkare urologi, Sahlgrenska Universitetssjukhuset och en av Mustaschkampens ambassadörer 2021:
Enbart PSA-testning ger överdiagnostik
– I våras försvarade jag min avhandling där jag undersökte vad magnetkameraundersökning kan bidra med i screening för prostatacancer då enbart PSA-testning inte är en tillräckligt bra metod. Fördelen med PSA-testning är att allvarlig prostatacancer kan upptäckas i ett tidigt skede och därmed öka chansen att bli botad. Nackdelen med PSA-provtagning är så kallad överdiagnostik; att prostatacancer som aldrig skulle ha utvecklats till en allvarlig sjukdom också hittas.
Vid Socialstyrelsens senaste bedömning 2018 ansågs inte att fördelen med regelbunden provtagning av PSA med minskad dödligheten i prostatacancer övervägde nackdelarna och därmed rekommenderades inte allmän screening för prostatacancer med PSA-testet. För att rekommendera screening för prostatacancer behövs alltså metoder som bättre kan skilja mellan betydelsefull/behandlingskrävande och betydelselös/icke-behandlingskrävande former av prostatacancer.
Röntgenläkarens erfarenhet har betydelse för magnetkamerans träffsäkerhet
– Min avhandling baserades till stor del på Göteborg 2-studien och visade att hälften av 50–60-åriga män som inbjudes till en screeningstudie för prostatacancer med PSA-prov och magnetkameraundersökning väljer att delta samt att magnetkameraundersökningens förmåga att upptäcka tumör i prostata varierade mellan olika röntgenläkare. Eftersom röntgenläkare som granskar många bilder vid enheter som gör många magnetkameraundersökningar har högre träffsäkerhet är det viktigt att kontinuerligt utvärdera kvaliteten av magnetkameraundersökning som metod.
Med träffsäkrare metod kan nyttan med prostatacancerscreening överväga skadan
– Just nu pågår analyser för att besvara Göteborg 2-studiens huvudfråga, nämligen om fördelarna/nyttan med screening för prostatacancer kan överväga nackdelarna/skadan när kombinationen PSA-prov och magnetkameraundersökning används som metod. Jag är också delaktig i Göteborg 2-studiens delstudie G2B-studien. Denna studie undersöker om biomarkörer i blodet kan öka träffsäkerheten vid screening så att såväl antalet män som behöver utredas med vävnadsprovtagning med risk för infektioner som överdiagnostiken minskar. Trots att det inte finns något nationellt program för prostatacancerscreening sker idag en utbredd PSA-testning bland män i Sverige. Det är visat att organiserad PSA-testning ökar jämlikheten och minskar dödligheten i prostatacancer mer än ostrukturerad PSA-testning. Därför erbjuds män i Västra Götaland organiserad prostatacancertestning. Detta projekt kommer också att bidra till att öka kunskapen om olika screeningtesters träffsäkerhet. Jag har goda förhoppningar om att de kommande årens forskningsresultat kommer att belysa hur män på ett optimalt sätt kan screenas för prostatacancer.
Mer information om aktuella forskningsprojekt finns på Prostatacancerförbundets webbplats






