Farmakologisk behandling vid cancerrelaterad smärta – så skräddarsyr du behandlingen till patienten
Webinar, 22 april 2020, 12:10 – 12:50
En föreläsning av Staffan Lundström, Docent, överläkare Palliativ vård och FoUU-enheten, Stockholms Sjukhem
Att lindra smärta hos patienter med spridd cancersjukdom kan vara en utmaning. En mekanismbaserad behandlingsstrategi är en god grund för en lyckad smärtbehandling och ger vägledning i valet av farmakologisk behandling. Staffan Lundström är specialist i onkologi, smärtlindring och palliativ medicin och ger i den här föreläsningen konkreta råd kring smärtbehandling vid cancersjukdom.
Iscaff Pharma – ny plattform för cancerdiagnostik och test av läkemedel

Iscaff Pharma AB är ett bioteknikföretag som fokuserar på att utveckla bättre behandlingar av aggressiva cancerformer. Det bygger på forskning av professor Göran Landberg och docent Anders Ståhlberg vid Sahlgrenska Cancer Center, Göteborgs universitet. Forskningen har dokumenterat att tumörens ställning (miljö) påverkar cancerns aggressivitet.
Nu har man utvecklat denna teknik till en kostnadseffektiv plattform för att förbättra framgången i klinisk utveckling av behandlingar mot aggressiv cancer. Studier vid Göteborgs universitet visar att delar av den tumörvävnad som normalt kasseras vid cancerkirurgi bär på hittills outnyttjad kunskap om sjukdomen.
Forskningen utgör grund för en ny experimentell plattform för cancerdiagnostik, prognoser och test av cancerläkemedel, som kommersialiseras inom Iscaff Pharma AB.
Forskarna berättar om sin forskning i en artikel som har publicerats på Sahlgrenska Akademins hemsida (se länk: https://sahlgrenska.gu.se/forskning/aktuellt/nyhet/ny-plattform-for-cancerdiagnostik-och-test-av-lakemedel.cid1676892)
URKLIPP:
Delar av den tumörvävnad som normalt kasseras vid cancerkirurgi bär på hittills outnyttjad kunskap om sjukdomen, visar studier vid Göteborgs universitet. Forskningen utgör grund för en ny experimentell plattform för cancerdiagnostik, prognoser och för att testa cancerläkemedel.
Den studie som forskargruppen hittills publicerat, i tidskriften Biomaterials, gäller bröstcancer. Pågående studier på bland annat tjocktarmscancer och äggstockscancer visar också positiva resultat för den nya tekniska plattformen och strategin.
Vid traditionell diagnostik efter cancerkirurgi är det tumörceller i den bortopererade vävnaden som undersöks. Beroende på cancerform görs mer eller mindre omfattande molekylära analyser, och undersökningar av prognosgener.
För bröstcancerpatienterna i den aktuella studien gjordes detta enligt rutin. Forskarna gick sedan vidare med den nya tekniken, i de fall det fanns borttagen tumörvävnad kvar att arbeta med. Istället för att titta på tumörceller studerades den stödjande struktur, av bland annat proteinfibrer, som omger cellerna och styr vävnadens uppbyggnad. Ett slags omgivande skelett.
Kunde förutsäga återfall
Anders Ståhlberg, docent i molekylär medicin, är en av två huvudansvariga för studien och plattformen:

– I vanliga fall undersöker man tumörceller och gör sig av med resten, här gör vi tvärtom. Det vi tittar på är cellernas omgivning, deras omgivningsskelett, och vi såg tidigt att det fanns stora skillnader mellan tumörer från olika patienter, som bara kunde upptäckas vid analys av dessa omgivningar, säger han.
Forskarna kunde bland annat förutsäga risken för återfall i bröstcancer genom att studera egenskaperna hos omgivningsskelettet i olika patienters vävnader. Detta skedde genom att man satte in identiska cancercellinjer i skeletten, och jämförde de olika utfallen.

Göran Landberg är professor i patologi och den andra drivande personen bakom forskningen:
– Våra resultat har tydliga kopplingar till kliniska parametrar, exempelvis hur aggressiv en tumör visade sig vara. Vi arbetar nu med att ta reda på vilka delar av cellernas omgivningsskelett som påverkade vad. Tekniken fungerar, och vi har kunnat visa att det här är en väldigt bra experimentell plattform med stor klinisk potential, säger han.
Testning av läkemedel
Utöver diagnostik och prognoser för hur en cancer ska utvecklas ser forskarna testning av läkemedel som ett viktigt område för den nya plattformen. En läkemedelskandidat kan då testas i flera olika individers bortopererade vävnad, för att se hur den potentiellt kan fungerar i olika patienter med cancer.
Syftet med plattformen är att testa vilka patienter som har nytta av en behandling innan den ges till människor. En annan fördel med den nya tekniken är att användningen av försöksdjur kommer att kunna minskas.
Göran Landberg och Anders Ståhlberg tillhör Sahlgrenska akademin, Göteborgs universitet, och Wallenbergcentrum för molekylär och translationell medicin. Viktig partner i studien är statliga forskningsinstitutet Rise, Research Institutes of Sweden AB och del av forskningen har varit finansierad av VINNOVA inom ett UDI-projekt (Utmaningsdriven Innovation) tillsammans med ett tiotal fler partners.
Venclyxto EU-godkänt i kombinationsbehandling vid KLL
AbbVie får godkänt från Europeiska kommissionen för Venclyxto (venetoklax) i kombinationsbehandling för patienter med obehandlad kronisk lymfatisk leukemi

- Venclyxto plus obinutuzumab är den första kemofria, tidsbestämda kombinationsbehandlingen, som har godkänts av Europeiska kommissionen för patienter med tidigare obehandlad kronisk lymfatisk leukemi (KLL)
- Godkännandet baseras på fas III-data från CLL14-studien, som visade att patienter som behandlades med obinutuzumab plus ett års behandling med Venclyxto hade en förlängd progressionsfri överlevnad (PFS) och högre andel patienter uppnådde icke-mätbar kvarvarande sjukdom jämfört med patienter som fick behandling med obinutuzumab plus klorambucil 1,5
AbbVie, ett forskande biopharmaföretag, meddelar att Europeiska kommissionen har godkänt Venclyxto i kombination med obinutuzumab för behandling av tidigare obehandlade KLL-patienter. Godkännandet gäller för alla 27 medlemsstaterna i EU liksom Island, Liechtenstein, Norge och Storbritannien.
− Godkännandet understryker den ökande nyttan av Venclyxto vid KLL-behandling och visar på dess kliniska värde som en kemofri kombinationsbehandling för tidigare obehandlade KLL-patienter i Europa, säger Neil Gallagher, läkare, PhD, ansvarig för läkemedelsutveckling på AbbVie. Vi ser fram emot att tillhandahålla Venclyxto till ännu fler patienter, som potentiellt kan ha nytta av att uppnå en djup respons och bibehållen progressionsfri överlevnad, med det extra värdet av att behandlingen är tidsbestämd.
Detta är det tredje godkännandet för Venclyxto, som är den första B-cellslymfom-2- (BCL-2) hämmaren. BCL-2 är ett protein som förhindrar cancerceller från att genomgå en programmerad celldöd, apoptos. Venclyxto är sedan tidigare godkänd för behandling i kombination med rituximab av vuxna KLL-patienter, som fått minst en tidigare behandling, samt i monoterapi för vuxna KLL-patienter med 17p-deletion eller TP53-mutation som är olämpliga för eller som har sviktat på en hämmare av B-cellsreceptorns signalväg eller hos vuxna patienter utan 17p-deletion eller TP53-mutation efter terapisvikt på både kemoimmunterapi och en hämmare av B-cellsreceptorns signalväg.
− KLL är vanligast bland de 95 000 som diagnosticeras med leukemi i Europa varje år, och kemoterapi är oftast den första behandlingen för dessa patienter säger Michael Hallek, läkare och ordförande för den tyska KLL-studiegruppen, direktör för avdelningen för internmedicin och centret för integrerad onkologi vid Kölns universitetssjukhus i Tyskland, samt studiens huvudprövare. Möjligheten att använda en kemofri kombinationsbehandling, som kan ge en djup respons och göra det möjligt att avsluta behandlingen, kommer att förändra sättet som vi behandlar KLL och medföra en betydande inverkan för patienterna.
Det senaste godkännandet baseras på resultat från primäranalysen (uppföljningstid 28 månader i median) av den kliniska fas III-studien CLL14, som visade en förlängd prövarbedömd progressionsfri överlevnad (PFS; behandlingstid utan sjukdomsprogression eller dödsfall) hos patienter som behandlades med Venclyxto plus obinutuzumab jämfört med klorambucil plus obinutuzumab (hazard ratio [HR]: 0,35, 95 % konfidensintervall [CI]: 0,23, 0,53; P <0,0001, median ännu inte nådd). Vid en uppdaterad effektanalys av CLL14 (uppföljningstid 40 månader i median) hade median PFS inte nåtts för Venclyxto plus obinutuzumab-armen, och var 35,6 månader (95 % konfidensintervall [CI]: 33,7, 40,7) i obinutuzumab plus klorambucil-armen (hazard ratio [HR]: 0,31, 95 % konfidensintervall [CI]: 0,22, 0,44). Beräknad PFS vid 36 månader för Venclyxto plus obinutuzumab var 81,9 % (95 % konfidensintervall [CI]: 76,5, 87,3) och var för obinutuzumab plus klorambucil 49,5 % (95 % konfidensintervall [CI]: 42,4, 56,6). Efter den avslutade ettåriga behandlingen, hade patienter med Venclyxtokombinationen uppnått en djup respons dvs högre andel av patienterna uppnådde icke-mätbar kvarvarande sjukdom (MRD-negativitet) eller komplett respons (CR) jämfört med de patienter som fick klorambucil plus obinutuzumab.1,5
Säkerhetsprofilen för kombinationen Venclyxto plus obinutuzumab överensstämde med den kända säkerhetsprofilen för vart och ett av läkemedlen. Minst en biverkan av varierande grad förekom hos 94,3 % av patienterna i Venclyxto kombinationsarmen. De vanligaste grad 3/4-biverkningarna var neutropeni och infektioner. Tumörlyssyndrom rapporterades hos tre patienter i Venclyxto plus obinutuzumab-armen (samtliga under obinutuzumab-behandlingen och före insättandet av Venclyxto).1
I januari 2020 meddelade AbbVie att Europeiska läkemedelsmyndighetens kommitté för humanläkemedel (CHMP) gett ett positivt utlåtande för godkännande för marknadsföring för Venclyxto i kombination med obinutuzumab för behandling av tidigare obehandlade KLL-patienter.
Om kronisk lymfatisk leukemi (KLL)
KLL är en långsamt växande form av leukemi, eller blodcancer, där för många omogna lymfocyter (en sorts vit blodkropp) förekommer, företrädesvis i blod och benmärg. I Europa nydiagnostiserades cirka 95 000 personer i leukemi under 2018.2 KLL är den vanligaste formen av leukemi i västvärlden och svarar för cirka en tredjedel av alla nydiagnostiserade leukemier.3,4
Om fas III-studien, CLL14
Den randomiserade, multicenter, öppna, kontrollerade fas III-studien CLL14, som genomfördes i nära samarbete med den tyska KLL-gruppen (DCLLSG), utvärderade effekt och säkerhet vid kombinationsbehandling med Venclyxto plus obinutuzumab (n=216) jämfört med obinutuzumab plus klorambucil (n=216) hos tidigare obehandlade KLL-patienter med samsjuklighet (total Cumulative Illness Rating Scale (CIRS) >6 eller kreatininclearance <70 ml/min). Behandlingarna administrerades under en tidsbestämd period om 12 månader för Venclyxto respektive klorambucil, båda i kombination med sex cykler av obinutuzumab. Studien omfattade 432 tidigare obehandlade patienter, som var diagnosticerade enligt kriterier från International Workshop on Chronic Lymphocytic Leukemia (iwCLL). Det primära effektmåttet var prövarbedömd PFS.1 Viktiga sekundära effektmått var MRD-negativitet i perifert blod och benmärg, samt total responsfrekvens (ORR) och komplett respons (CR).1
Om Venclyxto (venetoklax)
Venclyxto är det första i en helt ny klass av läkemedel, som selektivt binder till och hämmar proteinet B-cellslymfom-2 (BCL-2). Hos en del blodcancersjukdomar och andra cancersjukdomar anrikas BCL-2 och förhindrar naturlig celldöd, så kallad apoptos. Venclyxto är en målstyrd behandling som blockerar BCL-2, så att apoptosprocessen återställs och cancercellerna kan dö.
Venclyxto i kombination med obinutuzumab är avsett för behandling av vuxna patienter med tidigare obehandlad kronisk lymfatisk leukemi (KLL).5
Venclyxto i kombination med rituximab är avsett för behandling av vuxna patienter med KLL som fått minst en tidigare behandling.5
Venclyxto som monoterapi är avsett för behandling av KLL.5
- hos vuxna patienter med 17p-deletion eller TP53-mutation som är olämpliga för eller som har sviktat på en hämmare av B-cellsreceptorns signalväg, eller
- hos vuxna patienter utan 17p-deletion eller TP53-mutation efter terapisvikt på både kemoimmunterapi och en hämmare av B-cellsreceptorns signalväg.
Personer med hög tumörbörda kan under behandling med Venclyxto utveckla onormala nivåer av vissa kroppssalter (såsom kalium och urinsyra) i blodet på grund av att stora mängder cancerceller bryts ner snabbt. Detta kan leda till förändringar i njurfunktion, onormala hjärtslag eller krampanfall. Tillståndet kallas TLS (tumörlyssyndrom) och kan bli livshotande. Det finns risk för TLS under de första 5 veckorna av behandling med Venclyxto. Patienter ska alltid få förebyggande åtgärder, och finns det en ökad övergripande risk för TLS ska intensivare åtgärder sättas in.5
De vanligaste biverkningarna under behandling med Venclyxto är lågt antal vita blodkroppar (neutropeni), övre luftvägsinfektion, diarré, illamående, förstoppning och trötthet.5
Venclyxto utvecklas av AbbVie och Roche. Det marknadsförs gemensamt av AbbVie och Genentech, en medlem av Roche Group, i USA och av AbbVie utanför USA. Tillsammans, är de båda företagen dedikerade till forskning kring BCL-2, och Venclyxto prövas i flera kliniska studier inom flera blodcancersjukdomar och andra cancersjukdomar.
Venclyxto är godkänd i fler än 50 länder. AbbVie och Roche samarbetar förnärvarande med regulatoriska myndigheter I andra länder för att tillhandahålla denna behandling till fler behövande patienter.
För fullständig information om indikationer, kontraindikationer, varningar och försiktighet, biverkningar, pris och dosering, se Fass.se.
Referenser:
1. Fischer K, et al. Effect of fixed-duration venetoclax plus obinutuzumab (VenG) on progression-free survival (PFS), and rates and duration of minimal residual disease negativity (MRD–) in previously untreated patients (pts) with chronic lymphocytic leukemia (CLL) and comorbidities. Presented at the 2019 American Society of Clinical Oncology Annual Meeting: June 4, 2019; Chicago.
2. International Agency for Research on Cancer. World Health Organization. Europe Globocan 2018. https://gco.iarc.fr/today/data/factsheets/populations/908-europe-fact-sheets.pdf.Accessed February 2020.
3. NCI dictionary. NCI Dictionary of Terms. Chronic Lymphocytic Leukemia. https://www.cancer.gov/publications/dictionaries/cancer-terms. Accessed January 2020.
4.World Health Organization. 2014 Review of Cancer Medicines on the WHO List of Essential Medicines. http://www.who.int/selection_medicines/committees/expert/20/applications/CLL.pdf. Accessed January 2020.
5. Produktresumé för Venclyxto, www.fass.se
Acetylsalicylsyra kopplat till minskad levercancerrisk
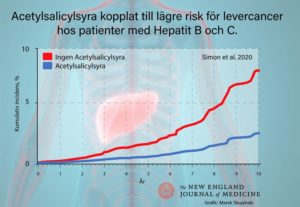
Vuxna med kronisk virushepatit och förhöjd risk för levercancer har lägre risk att drabbas av levercancer eller att dö av leversjukdom om de under lång tid medicinerat med acetylsalicylsyra (till exempel Trombyl) i låg dos. Det visar en studie som publiceras i tidskriften New England Journal of Medicine av forskare från Karolinska Institutet och Universitetssjukhuset Örebro i Sverige och Massachusetts General Hospital i Boston, USA.
– Levercancer och dödligheten i leversjukdom ökar i snabb takt i USA och Europa. Trots detta saknas etablerade behandlingar för att förhindra utvecklingen av levercancer eller för att minska risken för död i leversjukdom, säger studiens förstaförfattare Tracey Simon, forskare vid Massachusetts General Hospital.
I den aktuella studien analyserade forskarna data från 50 275 vuxna svenskar med kronisk virushepatit, en typ av leverinfektion som orsakas av hepatit B- eller C-virus. Dessa infektioner är den vanligaste riskfaktorn för levercancer. På tio år utvecklade 4,0 procent av patienterna som fick acetylsalicylsyra i låg dos (upp till 160 mg/dag) levercancer, jämfört med 8,3 procent av de som inte tog acetylsalicylsyra. Användningen av acetylsalicylsyra var kopplat till 31 procents lägre relativ risk för levercancer.
Ju längre en person tog acetylsalicylsyra, desto större var nyttan. Jämfört med kortvarig användning (tre månader till ett år) var risken för levercancer 10 procent lägre för personer som tagit acetylsalicylsyra i 1–3 år, 34 procent lägre för dem som tagit medicinen i 3–5 år och 43 procent lägre för dem som tagit medicinen i minst 5 år.
Dessutom var dödligheten i leversjukdom endast 11,0 procent hos dem som tagit acetylsalicylsyra jämfört med 17,9 procent av icke-användarna under en tioårsperiod, motsvarande 27 procents lägre relativ risk för dem som tagit medicinen.
Fördelarna av att äta acetylsalicylsyra sågs oberoende av kön, svårighetsgrad av leverinfektion eller typ av hepatitvirus (B eller C). Risken för inre blödningar (något som acetylsalicylsyra kan orsaka på lång sikt) var inte förhöjd bland personer som åt medicinen.

Jonas F. Ludvigsson, professor vid institutionen för medicinsk epidemiologi och biostatistik vid Karolinska Institutet och överläkare vid Universitetssjukhuset Örebro. Foto: Alexander Donka
– Detta är den första stora nationella studien som visar att användningen av acetylsalicylsyra är förknippad med en betydligt lägre långsiktig risk för levercancer och dödlighet i leversjukdom, säger studiens sisteförfattare Jonas F. Ludvigsson, professor vid institutionen för medicinsk epidemiologi och biostatistik vid Karolinska Institutet och överläkare vid Universitetssjukhuset Örebro.
Forskarna poängterar att randomiserade kliniska prövningar behövs för att ytterligare utreda fördelarna med acetylsalicylsyra för patienter med leversjukdom.
Forskningen finansierades av National Institutes of Health (USA), American Association for the Study of Liver Diseases, Boston Nutrition Obesity Research Council, Nyckelfonden, Region Örebro län och Karolinska Institutet. Se den vetenskapliga artikeln för fullständig redovisning om finansiering av alla medförfattare.
Publikation: “Association of Aspirin with Hepatocellular Carcinoma and Liver-Related Mortality”. Tracey G. Simon, Ann-Sofi Duberg, Soo Aleman, Raymond T. Chung, Andrew T. Chan, Jonas F. Ludvigsson. New England Journal of Medicine (NEJM), online 11 mars 2020, doi: 10.1056/NEJMoa1912035.
För mer information, kontakta:
Jonas F. Ludvigsson, professor, överläkare
Institutionen för medicinsk epidemiologi och biostatistik, Karolinska Institutet
Barnkliniken, Universitetssjukhuset Örebro
Tel: 019-602 1000
Mobil: 0730-296 318
E-post: [email protected]


