En ny lovande strategi för behandling av lungcancer har utvecklats av forskare vid Lunds universitet. Behandlingen kombinerar ett nytt kirurgiskt tillvägagångssätt med smarta nanopartiklar för att specifikt angripa lungtumörer. Den nya studien har publicerats i juliutgåvan av Advanced Therapeutics.
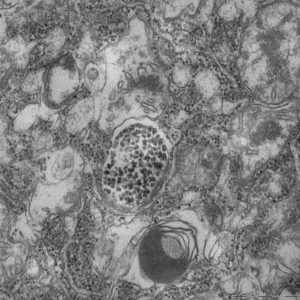
Nanopartiklar i lungtumörceller
Svårt att nå solida tumörer
Lungtumörer är ofta svåra att ta bort med nuvarande kirurgiska tekniker på grund av deras placering i lungan eller det faktum att det finns tumörer som är för små för att observera. Tumörerna utvecklar ofta naturliga barriärer för att förhindra att läkemedel och immunceller når in till tumörcellerna.

Darcy Wagner och Deniz Bölükbas
– Därför får patienter ofta höga doser kemoterapeutika (cellgifter) som cirkuleras genom hela kroppen och resulterar i stora biverkningar i andra organ. Ett antal nya behandlingar mot lungcancer har i studier visat sig lovande i labbet, men en stor utmaning har kvarstått: hur man levererar rätt läkemedel specifikt till dessa speciella tumörer som är svåra att nå, förklarar Darcy Wagner, docent och chef för forskningsgruppen.
Ny kirurgisk teknik
För att övervinna denna utmaning utvecklade forskarna bakom den nya studien: Bölükbas, Wagner med kollegor, forskare från gruppen Lung Bioengineering & Regeneration, en ny kirurgisk teknik som introducerar nanopartiklarna enbart i lungans blodkärl. Blodkärlen runt och i tumörer är annorlunda än i normala organ. Forskarna använde denna skillnad för att rikta nanopartiklar till de inre delarna av stora och täta solida lungtumörer. Bölükbas och kollegor använde djurmodeller som har ett komplett immunsystem och tumörer som liknar de typer av lungtumörer som patienterna har.
– Med hjälp av vår teknik, som vi kallar ”organ restricted vascular delivery” (ORVD), kunde vi hitta lungcancerceller med de introducerade nanopartiklarna inuti dem. Det har vi inte kunnat göra tidigare i dessa typer av djurmodeller för lungcancer, säger Deniz Bölükbas, postdok och studiens försteförfattare.
Förhindrar skador på friska celler
Dessutom konstruerades nanopartiklarna för att endast frisätta läkemedel på en specifik signal som finns i tumörområdet. Detta minskar risken för att läkemedlen i nanopartikeln orsakar skador i friska lungceller och kan möjliggöra att högre mängder giftiga läkemedel används för att öka antalet dödade tumörceller utan att orsaka oönskade biverkningar.
– Även om smarta nanopartiklar med unika egenskaper kan konstrueras på olika sätt, leder frisläppandet av dessa i blodomloppet ofta till en okontrollerad spridning av partiklarna, och det är endast ett fåtal av dem som når de inre delarna av de solida tumörerna. Detta har varit en global utmaning som har hindrat en mer utbredd användning av nanopartikelsystem inom sjukvården, säger Darcy Wagner.
Studien har letts av Deniz Bölükbas, postdoktor vid Wallenberg Molecular Medicine Fellow vid Lunds universitet och docenten Darcy Wagners forskningsgrupp. Wagner och hennes team fokuserar på att utforma nya behandlingar för patienter med lungsjukdomar genom att kombinera teknik, medicin och cellbiologi.- Detta är ett betydande steg framåt inom behandling av lungcancer, säger Bölükbas, men det är viktigt att potentialen i denna metod valideras.
Fakta/Lungcancer
Lungcancer är en av de dödligaste formerna av cancer, med en överlevnad på endast 15 procent. Förutom tumörer som ursprungligen bildas i lungan är lungan även en av de vanligaste platserna för metastaser. Många lungtumörer går inte att operera och det finns begränsade behandlingsalternativ. Med cirka 2 miljoner diagnoser och 1,8 miljoner dödsfall per år i världen, är behovet mycket stort av nya behandlingar mot lungcancer. I Sverige dog 3 593 personer över 15 år i lungcancer 2018.
Fakta/Samarbete över gränser
Studien bygger på starka samarbeten mellan experter från kompletterande forskningsområden. Medförfattare Silke Meiners, Helmholtz Center München: expert på cellulär dysregulation i lungsjukdomar, Thomas Bein: expert på syntes och karaktärisering av nanopartiklar, Georgios Stathopoulos: expert på lungcancer.
Bölükbas och Wagner inspirerades att testa sin teknik med ex vivo lung perfusion (EVLP) – en världsberömd upptäckt från Lunds universitets för att bevara, utvärdera och reparera donatorlungor för klinisk transplantation. Det var en unik möjlighet att samarbeta med docent Sandra Lindstedt, doktor, en kardiotorasisk transplantationskirurg vid Skånes universitetssjukhus och knuten till Wallenberg Center for Molecular Medicine på Lunds universitet. Lindstedt var doktorand i teamet som utvecklade denna teknik och använder EVLP för lungtransplantationspatienter vid Skånes universitetssjukhus.
Finansiering
Wagner och Bölükbas har fått stöd från Knut och Alice Wallenbergs Stiftelse (# PA2016-1522) och Åke och Inger Bergkvists Stiftelse för Darcy Wagner; Nanosystems Initiative München-stöd för Deniz Bölükbas, samt stöd från Center for NanoScience München, den tyska forskningsstiftelsen (SFB 749 och SFB 1032), Europeiska unionens program för forskning och innovation för Horizon 2020 (# 686098) och Europeiska forskningsrådet 2010 Starta Oberoende utredare och Proof of Concept Grants 2015 (# 260524 och #679345).
Länk till artikeln:
Organ‐Restricted Vascular Delivery: Organ‐Restricted Vascular Delivery of Nanoparticles for Lung Cancer Therapy (Adv. Therap. 7/2020)