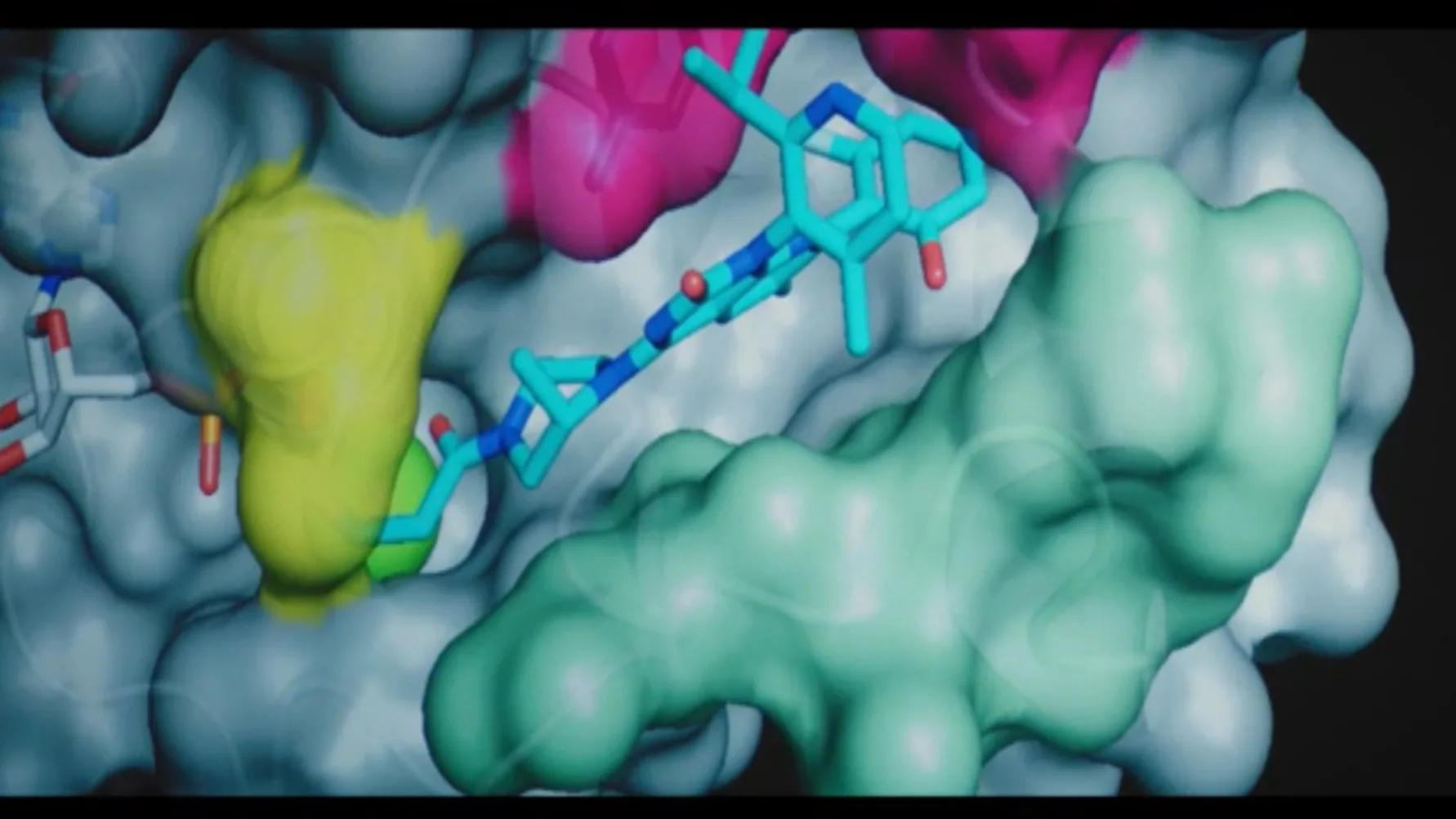
Lumykras (sotorasib) är en småmolekylhämmare som selektivt och irreversibelt binder till cystein 12 (C12) på det muterade KRAS G12C-proteinet.
Den europeiska läkemedelsmyndigheten EMA:s vetenskapliga nämnd, the Committee for Medicinal Products for Human Use (CHMP) rekommenderar EU-kommissionen att godkänna Lumykras (sotorasib) för behandling av patienter med avancerad KRASG12C-muterad icke-småcellig lungcancer som progredierat efter minst en linje av systemisk behandling.
– Om EU-kommissionen väljer att följa nämndens rekommendation innebär det att det för första gången kommer finnas en godkänd målriktad behandling för europeiska patienter som specifikt riktar sig mot denna relativt vanliga mutation, säger Sandra Eketorp Sylvan, medicinsk chef på Amgen Sverige.
CHMP grundar sitt positiva utlåtande på kliniska resultat som visar på ihållande respons och gynnsam nytta-riskprofil för Lumykras.
Icke-småcellig lungcancer, NSCLC, utgör över 80 procent av alla lungcancerfall (NSCLC = non-small-cell lung carcinoma). Mellan 13 och 15 procent av dessa har en mutation, KRASG12C, som leder till okontrollerad celldelning och som – hittills – inte varit möjlig att specifikt målrikta läkemedel mot. Patienter med KRASG12C-mutation som inte längre är hjälpta av första linjens behandling når, med de idag tillgängliga behandlingsalternativen, en progressionsfri överlevnad på cirka fyra månader.
Med Lumykras har Amgen lyckats med den utmaning som otaliga forskargrupper under de senaste fyra decennierna gått bet på, att ta fram en målriktad behandling som specifikt hämmar effekten av denna KRAS-mutation. Ett avgörande hinder har varit att KRAS-proteinet saknar naturliga fickor som en småmolekylhämmare kan binda till, men Amgen-forskarna fann en tidigare okänd räffla som Lumykras utnyttjar för att låsa det KRASG12C-muterade proteinet i ett inaktivt tillstånd vilket försämrar cancercellernas förmåga att dela sig och överleva.
CHMP grundar sitt positiva utlåtande på resultat från den kliniska fas II-studien CodeBreaK 100. I studien inkluderades 126 patienter med KRASG12C-muterad, avancerad NSCLC, varav 124 hade utvärderbara lesioner vid baslinjen. Lumykras uppvisade gynnsamma resultat både vad gäller effekt och tolerabilitet hos patienterna som alla progredierat på platinabaserad kemoterapi och/eller immunterapi med PD1/L1-hämmare.
Lumuykras, 960 mg, administrerat oralt en gång per dag, resulterade i en objektiv tumörrespons på 37,1 procent (ORR = Objective Response Rate) och fler än fyra av fem, 80,6 procent, uppnådde sjukdomskontroll (DCR = Disease Control Rate). ORR definierades i detta fall som andel patienter med ≥ 30-procentig minskning av summan av target-lesionens längsta diameter jämfört med baslinjen. Responsdurationen var i median 11,1 månader, progressionsfria medianöverlevnaden 6,8 månader, och den totala medianöverlevnaden (OS = Overall Survival) var 12,5 månader.
– Patienter med KRASG12C-muterad NSCLC som progredierat på första linjens behandling har en dyster prognos och många svarar inte på eller får för mycket biverkningar av de behandlingar som finns tillgängliga idag. Mot den bakgrunden skulle ett europeiskt godkännande av Lumykras vara ett välkommet behandlingsalternativ för de patienter som lever med denna relativt vanliga mutation, säger Sandra Eketorp Sylvan som själv är onkolog.
De vanligaste behandlingsrelaterade biverkningarna (TRAE = Treatment-Related Adverse Events) var diarré (32 procent), illamående (19 procent), förhöjt alaninaminotransferas (ALAT) respektive aspartataminotransferas (ASAT) (15 procent vardera). De vanligast förekommande allvarliga (grad ≥ 3) behandlingsrelaterade biverkningarna var förhöjt ALAT (6 procent), förhöjt ASAT (6 procent) och diarré (4 procent). Endast 7 procent avslutade behandlingen till följd av behandlingsrelaterade biverkningar.3
Detaljerade fas II-data från CodeBreaK 100 presenterades vid 2020 World Conference on Lung Cancer (WCLC) och finns publicerade i New England Journal of Medicine (NEJM).
Om KRAS
Närmare 40 år av forskning har visat att RAS-genfamiljen är en av de vanligaste muterade onkogenerna i solida tumörer (RAS = RAt Sarcoma virus). Inom denna familj är KRAS (Kirsten RAt Sarcoma virus) den vanligaste varianten och är särskilt ofta förekommande i solida tumörer. Den beräknade incidensen av den specifika mutationsvarianten KRASG12C är cirka 13–15 procent vid icke-småcellig lungcancer, 3–5 procent vid kolorektalcancer och en till två procent vid många andra solida tumörer. KRASG12C har hittills inte betraktats som ett möjligt mål för läkemedel då proteinet saknar naturliga fickor som en småmolekylhämmare kan binda till.
Om CodeBreaK
Det kliniska studieprogrammet CodeBreaK för sotorasib är utformat för att behandla flera olika KRASG12C-muterade solida tumörer i hopp om att möta de ouppfyllda medicinska behov som länge förelegat vid dessa cancerformer.
CodeBreaK 100 är en fas I och II first-in-human, oblindad multicenterstudie som enrollerat patienter med KRASG12C-muterade solida tumörer. Patienter som bedömdes lämpliga var tungt förbehandlade och hade genomgått minst två tidigare behandlingslinjer.
Det primära effektmåttet i fas I-studien är säkerhet. Viktiga sekundära effektmått inkluderar objektiv tumör-respons (ORR = Objective Response Rate) bedömd var sjätte vecka, responsduration (DOR = Duration of Response) och progressionsfri överlevnad. Patienterna delades in i fyra doskohorter, 180 mg, 360 mg, 720 mg och 960 mg. Sotorasib administreras peroralt en gång om dagen i samtliga kohorter.
Det primära effektmåttet i fas II-studien var centralt utvärderad objektiv tumörrespons (ORR = Objective Response Rate). En global randomiserad fas III-studie, CodeBreaK 200, jämför sotorasib med docetaxel.
Mer information om CodeBreaK-programmet finns på www.hcp.codebreaktrials.com.
Om Lumykras (sotorasib)
Lumyras (sotorasib) är en first-in-class småmolekylhämmare som specifikt och irreversibelt binder till KRASG12C via den cysteinaminosyra som ersätter glycin när mutationen inträffar. KRASG12C blir på så vis låst i ett inaktivt GDP-bundet tillstånd (GDP = guanosine diphosphate, guanosindifosfat). Detta är möjligt efter att forskarna bakom Lumyras upptäckt en tidigare dold ”räffla” på KRASG12C-proteinet.