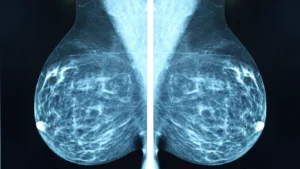
I den aktuella studien skapade forskarna en AI-modell som tränats till att analysera mammografibilder.
I ett projekt vid Lunds universitet tränas en AI-modell till att hitta de bröstcancerpatienter som kan avstå ingrepp i armhålan. Modellen analyserar tidigare outnyttjad information i mammografibilder, och ringar med hög träffsäkerhet in den individuella risken för metastaser i armhålan. I en nyligen avslutad studie visar modellen att drygt 40 procent av dagens armhåleingrepp skulle kunna undvikas.
Vid bröstcancer undersöks lymfkörtlarna i armhålan (så kallade axillära lymfkörtlar) för att bedöma prognos och val av behandling. En liten operation görs, där de första lymfkörtlarna identifieras och opereras bort för analys. Ingreppet är litet men kan ge smärta, svullnad, känselpåverkan och ibland vätskeansamling. Ungefär var femte patient med bröstcancer har spridning till armhålan. Hos övriga cirka 80 procent är lymfkörtlarna fria från cancer. Då är ingreppet enbart diagnostiskt, utan behandlande effekt.
– I den aktuella studien har vårt fokus legat på att förutse risken för metastaser i armhålan, berättar Lisa Rydén, professor i kirurgi vid Lunds universitet och överläkare vid Skånes universitetssjukhus.
Stort forskningsfokus läggs på att hitta icke-invasiva diagnostiska metoder som tidigare än idag kan berätta om lymfkörtlarnas status. Lisa Rydén är ansvarig för forskningsprojektet NILS (Non-invasive lymph node staging), ett flerårigt forskningssamarbete mellan den medicinska och den naturvetenskapliga fakulteten vid Lunds universitet.
– I dag görs ett separat ingrepp i armhålan, så kallad portvaktskörtelbiopsi, för att bedöma spridning till lymfkörtlar. Med NILS som utgångspunkt skulle vi i stället, utifrån patient- och tumördata, kunna göra en mer individbaserad riskbedömning redan före operationen. Om risken är låg skulle en operation i armhålan, i dialog med patienten, kunna avstås. Om den är hög skulle vi planera för kirurgi. Det skulle vara ett steg mot mer personcentrerad vård där varje åtgärd har tydlig nytta för just den patienten, säger Lisa Rydén.
I studien skapade forskarna en AI-modell som tränats till att analysera mammografibilder. Mammografibilderna tas rutinmässigt i samband med bröstcancersjukdom, och innebär alltså ingen extra åtgärd eller kostnad. Bilder från 1265 skånska kvinnor, diagnosticerade med bröstcancer mellan 2009 och 2017, användes. Gemensamt för studiedeltagarna var att deras bröstcancer befann sig i ett tidigt skede och att kirurgi var den första behandlingen. Resultaten av studien har publicerats i den vetenskapliga tidskriften NPJ Digital Medicine.
AI-modellen tränades till att identifiera olika slags information – från hela mammografibilden, inte bara den del som visade tumören. Det är utifrån denna komplexa information som modellen sedan kunnat räkna ut risken för metastaser.
– Vi utvecklade vår algoritm i tre steg. Först fick AI-modellen bland tiotusentals mammografibilder lära sig deras grundstruktur, som kanter, textur och former. Sedan tränades den att hitta särskilda ledtrådar till cancer, såsom tumörens gränser. Till sist fick den ett ”helhetstänk” genom att ta med annan viktig patientinformation, som ålder och tumörtyp, för att mer korrekt kunna förutsäga metastasrisken, säger Daqu Zhang, doktorand vid Naturvetenskapliga fakulteten, Lunds universitet.

Medlemmar i NILS-projektet, från vänster: Looket Dihge, Medicinska fakulteten, Patrik Edén, Naturvetenskapliga fakulteten, Lisa Rydén, Medicinska fakulteten och Daqu Zhang, Naturvetenskapliga fakulteten. Foto: Ingemar Hultquist
AI-modellen användes för att klassificera lymfkörtlarna som sjukdomsfria eller inte, och forskarna kunde visa att portvaktskörtelbiopsi skulle ha kunnat undvikits i 41,7 procent av fallen.
– Den här studien pekar på att man genom att använda AI-modellen i stället för att operera alla patienter kan vi ringa in dessa drygt 40 procent av patienterna där man kan avstå från ingreppet, förklarar Lisa Rydén.
Sverige sticker ut internationellt med den täta, allmänna bröstscreening som erbjuds här. Runt 67 procent av de svenska bröstcancerfallen upptäcks vid mammografiscreening hos kvinnor mellan 40 och 74 år. Kallelser till undersökning går ut med 18 till 24 månaders mellanrum, beroende på kvinnans ålder.
– I många länder saknas sådan populationsbaserad screening. För att kunna hävda att våra resultat är allmängiltiga, behöver vi få dem validerade, alltså bekräftade, på ett oberoende sätt. Så nu söker vi med ljus och lykta efter ett sådant oberoende patientmaterial både i Sverige och utomlands, säger Lisa Rydén.
Hon hoppas att AI-modellens inbyggda beräkningsalgoritmer i framtiden kan användas till att redan vid mammografiundersökningen bedöma risken för lymfkörtelmetastaser. Och att behandlingen då genast kan utformas utifrån denna risk.
– I ett drömscenario skulle man kunna få mycket mer information om tumörstadium och prognos från de diagnostiska mammografibilderna. Vår artikel fokuserar på spridning till lymfkörtlarna, men i pågående internationella studier kan bildmönstret även förutse prognos, säger Lisa Rydén.
Kortfakta om studien:
Tvärvetenskaplig forskning// peer review-granskad publikation// kohortstudie//antal patienter i studien: 1265 // statistiska samband // retrospektiv
Publikation
Deep learning on routine full-breast mammograms enhances lymph node metastasis prediction in early breast cancer, NPJ Digital Medicine, 2025
DOI:10.1038/s41746-025-01831-8
Finansiering
Erling Perssons Stiftelse, Sjöbergstiftelsen, Alf och Vetenskapsrådet.







